Учёные начали контроллировать "живчиков".
Исследователи создали биогибридных микророботов, покрыв сперматозоиды магнитными наночастицами. Таких «киборгов» направляли с помощью магнитных полей и впервые рентгеном отслеживали их положение внутри модели человеческого тела. Это открывает новые перспективы для лечения бесплодия и целевой доставки лекарств.
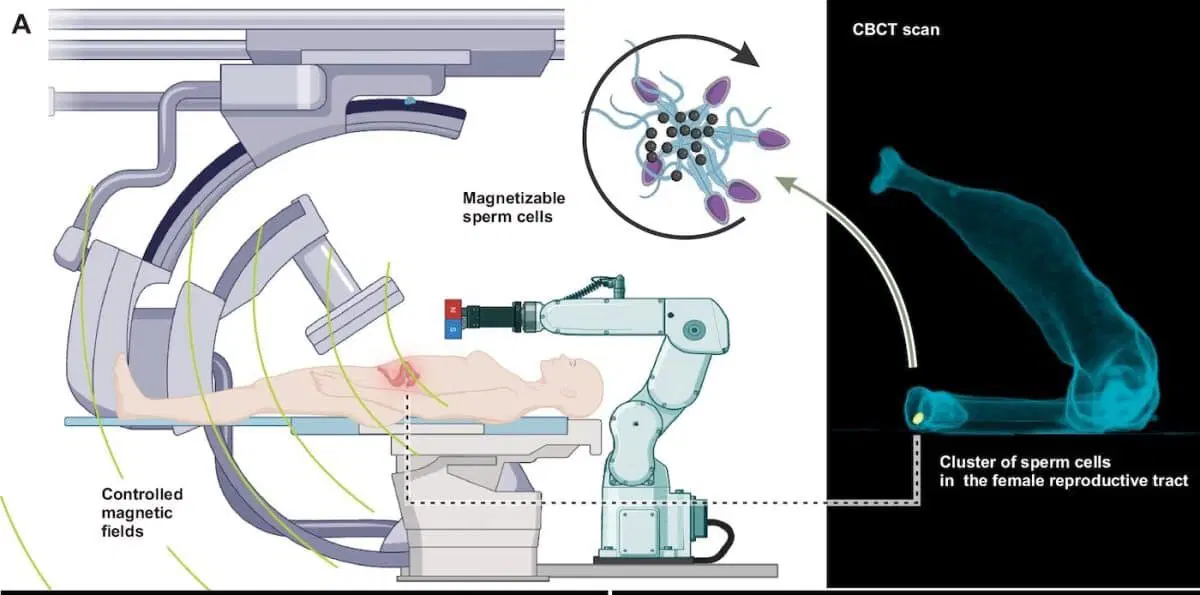
Сперматозоиды обладают уникальными природными способностями. Это эффективные и быстрые пловцы, приспособленные для навигации в сложной среде женской репродуктивной системы. Благодаря таким качествам они стали перспективными кандидатами для создания медицинских микророботов, способных доставлять лекарства или выполнять другие задачи внутри организма.
Основная проблема, которая мешала их использованию, — невидимость. Сперматозоиды слишком малы, имеют низкую плотность и почти прозрачны для рентгеновских лучей. Поэтому отследить их движение внутри тела с помощью стандартных неинвазивных методов было невозможно. Существующие оптические подходы либо требовали хирургического вмешательства, либо были ограничены малой глубиной проникновения, что не подходит для изучения процессов в человеческом организме.
Команда ученых из Нидерландов и Канады нашла решение этой проблемы. Результаты опубликованы в журнале npj Robotics. Исследователи использовали неживые бычьи сперматозоиды, которые послужили биологической основой для микророботов
.Сначала клетки сгруппировали в кластеры, затем покрыли их
наночастицами оксида железа. Этот процесс основан на электростатическом
самособирании — частицы сами притягиваются к поверхности сперматозоидов.
Наночастицы выполняют сразу две функции: делают кластеры восприимчивыми
к внешним магнитным полям и достаточно плотными для поглощения
рентгеновского излучения. Готовых микророботов поместили в заполненную
жидкостью анатомическую модель женской репродуктивной системы,
напечатанную на 3D-принтере.
Для управления роботами задействовали роботизированный манипулятор с
постоянным магнитом. Он создавал вращающееся магнитное поле, которое
заставляло кластеры катиться вдоль внутренних поверхностей модели. Так
впервые удалось одновременно управлять движением биороботов и
отслеживать их перемещение в реальном времени с помощью рентгеновской
флюороскопии.
Во время испытаний микророботы продемонстрировали высокую
управляемость. Их успешно провели по всей модели: от шейки матки через
ее полость до правой или левой маточной трубы. Весь путь занимал менее
50 секунд. Скорость движения кластеров зависела от частоты вращения
магнитного поля. При увеличении частоты от двух до 10 герц средняя
скорость роботов возрастала до 8-12 миллиметров в секунду. Дальнейшее
увеличение частоты приводило к тому, что кластеры начинали распадаться
на более мелкие части.
Исследователи протестировали три разные концентрации магнитных наночастиц: один, два и три миллиграмма на миллилитр. Все они оказались достаточными как для надежного управления, так и для четкой визуализации с помощью рентгена. Также проверили биосовместимость роботов. Кластеры в течение 72 часов контактировали с культурой клеток эндометрия человека. Тесты показали, что они не вызывают значительной токсичности — жизнеспособность клеток сохранялась на уровне от 74% до 88%.
Эта работа показала принципиальную возможность создания управляемых и
видимых внутри тела биороботов на основе сперматозоидов. В будущем
такая технология может привести к разработке новых методов целевой
доставки лекарств для лечения заболеваний матки или маточных труб,
например эндометриоза, миомы или рака.
Тем не менее технология находится на самом раннем этапе развития, до
ее клинического применения еще далеко. Эксперименты проводили в жесткой
пластиковой модели, которая лишь имитировала анатомию, но не
воспроизводила сложную среду живого организма с его мягкими тканями,
потоками жидкости и иммунной системой.
Распад кластеров на части при движении остается серьезной проблемой.
Таким образом, рассуждения о лечении реальных заболеваний с помощью
таких роботов пока остаются умозрительными


Комментарии